總 ORR 87.5%!邁威生物 9MW2821 2025 ASCO 口頭報告回顧
重要新聞
5 月 30 日 - 6 月 3 日在美國芝加哥舉辦的 2025 美國臨床腫瘤學(xué)會(huì )年會(huì )(ASCO)上,9MW2821 與特瑞普利單抗聯(lián)合用于治療局部晚期或轉移性尿路上皮癌(la/mUc)患者的 Ib/II 期臨床研究結果由北京大學(xué)腫瘤醫院泌尿腫瘤內科主任醫師盛錫楠教授代表研究團隊進(jìn)行了報告。9MW2821 聯(lián)合特瑞普利單抗在尿路上皮癌展現了令人鼓舞的療效及良好的安全性。
口頭報告
研究背景:
尿路上皮癌(UC)是世界范圍內常見(jiàn)的惡性腫瘤。2024 年發(fā)布的全球癌癥統計報告中顯示,膀胱癌是全球第九大常見(jiàn)診斷的癌癥,每年有新發(fā)病例約 61.4 萬(wàn),死亡病例約 22.0 萬(wàn)。男性疾病負擔和發(fā)病率顯著(zhù)高于女性,膀胱癌是男性第六大常見(jiàn)癌癥,是男性癌癥死亡第九大原因[1]。
9MW2821 (Bulumtatug Fuvedotin, BFv) 是新一代靶向 Nectin-4 的抗體偶聯(lián)藥物,早期研究顯示 9MW2821 在既往接受過(guò)含鉑化療和免疫檢查點(diǎn)抑制劑的局部晚期或轉移性尿路上皮癌人群中展現了具有潛力的療效[2]。單藥末線(xiàn)的 III 期關(guān)鍵臨床正在進(jìn)行中(NCT06196736,CTR20234024)。
特瑞普利單抗(Toripalimab)是一種新型人源化重組抗 PD-1 單抗,已先后在中美等多國獲批上市。
本次 ASCO 會(huì )議首次詳細匯報了 9MW2821 聯(lián)合特瑞普利單抗在局部晚期或轉移性尿路上皮癌患者中療效和安全性。
研究方法:
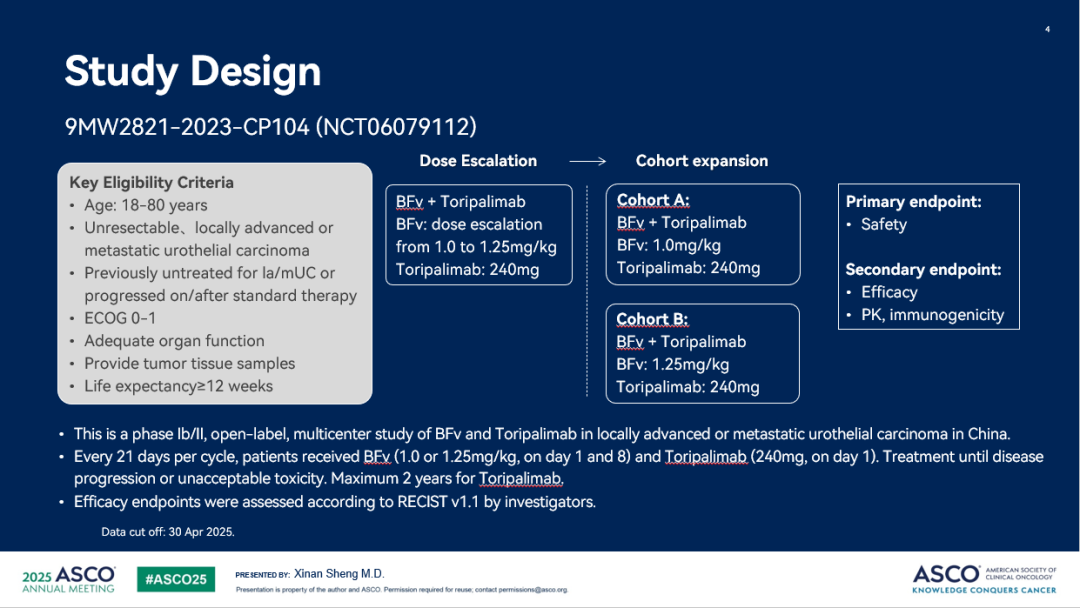
本研究是一項開(kāi)放、多中心的 Ib/II 期臨床試驗,篩選合格的受試者將接受 9MW2821 聯(lián)合特瑞普利單抗治療。特瑞普利單抗采用固定給藥劑量 240mg,在劑量遞增階段 9MW2821 從 1.0mg/kg 遞增至1.25mg/kg,在隊列擴展階段將分別在 1.0mg/kg 和 1.25mg/kg 劑量組進(jìn)行擴展。每 21 天 1 個(gè)周期,9MW2821 每周期 D1 和 D8 各給藥一次,特瑞普利單抗每周期 D1 給藥一次,直至發(fā)生疾病進(jìn)展或不可耐受的毒性。
研究結果:
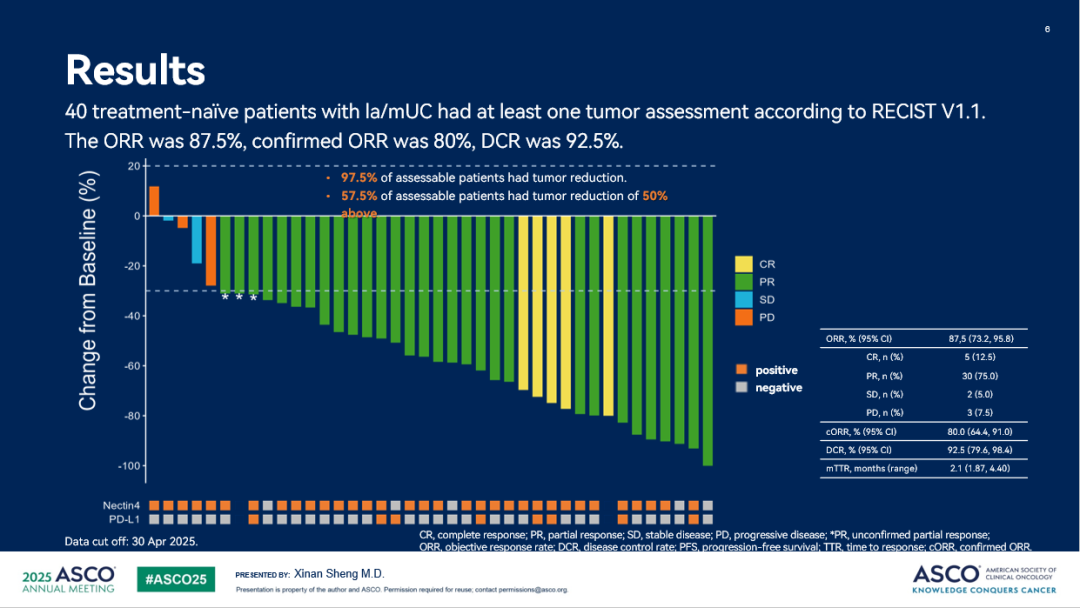
截至 2025 年 4 月 30 日,本研究共入組 52 例局部晚期或轉移性尿路上皮癌(la/mUC)受試者。40 例可腫評的晚期 UC 一線(xiàn)受試者中,中位年齡 67 歲,70% 為男性,72.5% ECOG 評分為 1 分,腫瘤原發(fā)部位為上尿路的占比 55%,肝轉移占比 15%。生物標志物表達方面,82.5% 為 Nectin-4 表達陽(yáng)性,20% 為 PD-L1 表達陽(yáng)性。
研究結果顯示,客觀(guān)緩解率(ORR)為 87.5%(95% CI: 73.2,95.8),經(jīng)確認的 ORR 為 80%,CR 率為 12.5%。疾病控制率(DCR)為92.5%(95% CI: 79.6,98.4)。最佳靶病灶大小變化與基線(xiàn)相比,97.5% 的受試者腫瘤病灶縮小,57.5% 的受試者腫瘤縮小超過(guò) 50%。
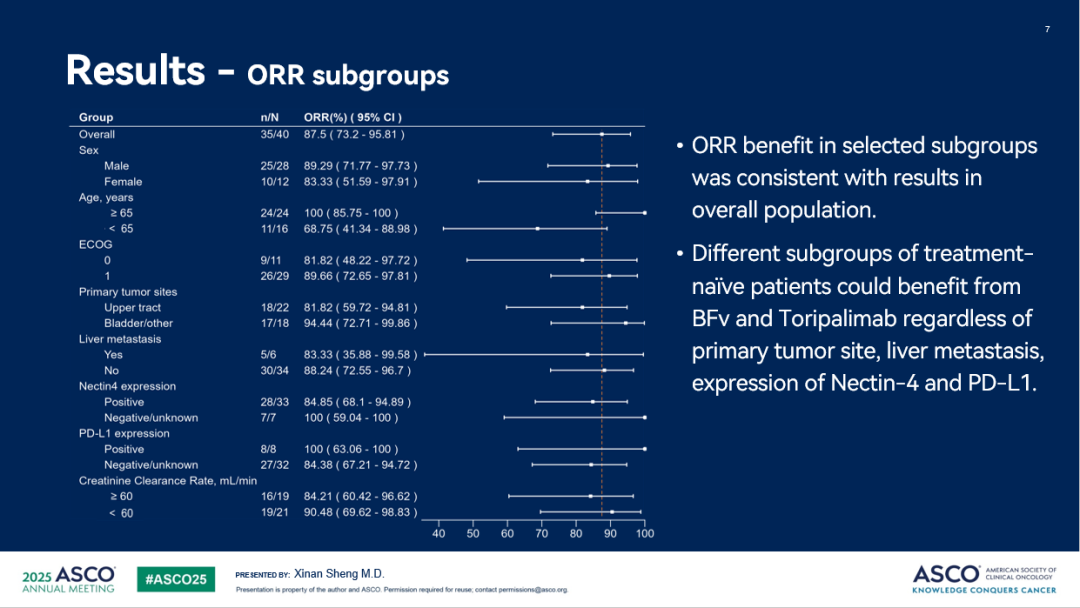
ORR 亞組分析顯示,在選定的亞組中,ORR 獲益與總體人群保持一致。無(wú)論年齡、腫瘤原發(fā)部位、是否基線(xiàn)存在肝轉移、以及腫瘤生物標志物 Nectin-4 和 PD-L1 的表達狀態(tài),所有亞組均可從 9MW2821 聯(lián)合特瑞普利單抗的治療中獲益。年齡超過(guò) 65 歲、腫瘤原發(fā)部位為下尿路、肝轉移、Nectin-4 表達陰性以及 PD-L1 表達陽(yáng)性的受試者 ORR 分別為100%(24/24)、94.44%(17/18)、83.33%(5/6)、100%(7/7)、100%(8/8)。
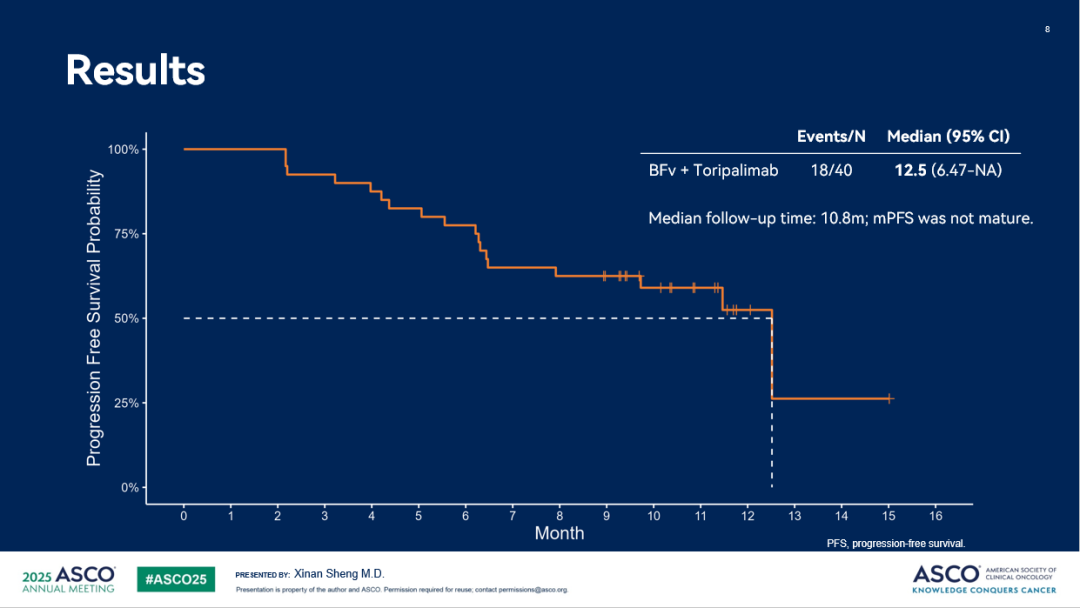
截至 2025 年 4 月 30 日,45% (18/40) 受試者發(fā)生疾病進(jìn)展或死亡,中位無(wú)進(jìn)展生存期(mPFS)為 12.5 個(gè)月(95% CI:6.47-NA),中位緩解持續時(shí)間(mDoR)尚未達到。中位隨訪(fǎng)時(shí)間為 10.8 個(gè)月,mPFS 和 mDoR 尚未成熟。
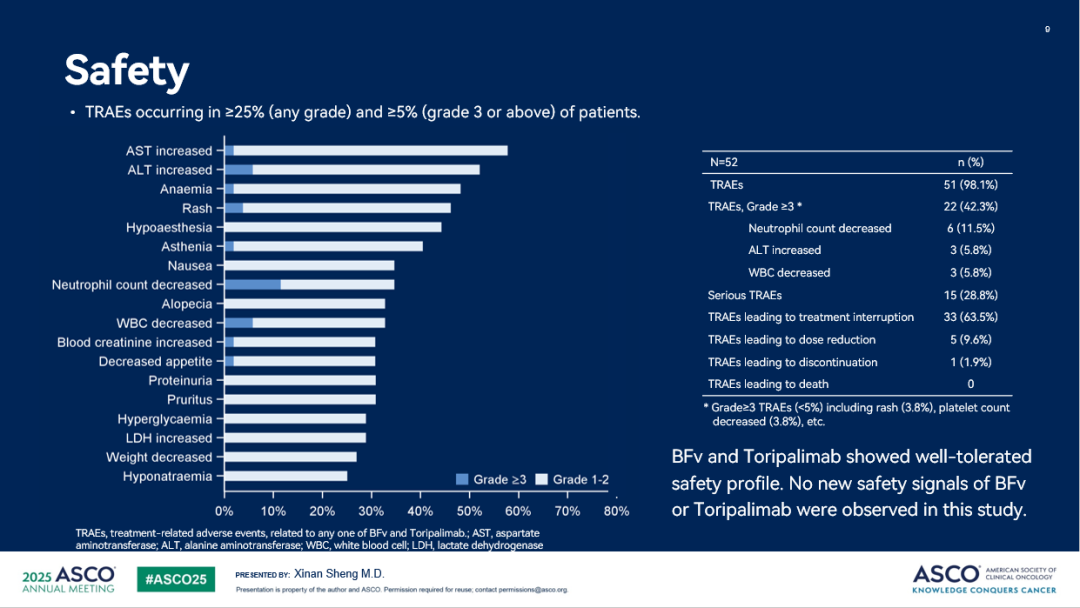
安全性方面,治療相關(guān)不良事件(TRAE)發(fā)生率為 98.1%,絕大多數 TRAE 為 1-2 級;3級及以上TRAE 發(fā)生率為 42.3%,≥3 級的 TRAE 主要表現為中性粒細胞計數降低(11.5%)、ALT 升高(5.8%)、白細胞計數降低(5.8%)等;治療相關(guān)嚴重不良事件的發(fā)生率為 28.8%,未發(fā)生導致死亡的 TRAE。聯(lián)合治療過(guò)程中,受試者整體耐受性良好,未觀(guān)察到新的安全性信號。
結論:
9MW2821 聯(lián)合特瑞普利單抗治療局部晚期或轉移性尿路上皮癌展現出了令人鼓舞的療效及良好的安全性特征。值得注意的是,本研究中高齡、肝轉移以及生物標志物 Nectin-4 表達為陰性的受試者也均取得了相當可觀(guān)的療效緩解,預示著(zhù)相較于傳統含鉑化療,9MW2821 聯(lián)合特瑞普利單抗將為那些不能耐受含鉑化療或潛在化療預后差的晚期尿路上皮癌患者提供新的治療選擇,有望成為真正意義上的、可覆蓋全部晚期尿路上皮癌人群的新療法。9MW2821 聯(lián)合特瑞普利單抗對比含鉑化療治療一線(xiàn)晚期尿路上皮癌的 III 期關(guān)鍵注冊臨床研究正在進(jìn)行中(NCT06592326,CTR20242828)。
關(guān)于 9MW2821
9MW2821 是由邁威生物自主研發(fā)的靶向 Nectin-4 ADC 創(chuàng )新藥,通過(guò)具有自主知識產(chǎn)權的偶聯(lián)技術(shù)連接子及優(yōu)化的 ADC 偶聯(lián)工藝,實(shí)現抗體的定點(diǎn)修飾。該品種是國內同靶點(diǎn)藥物中首個(gè)開(kāi)展臨床試驗的品種,亦是全球同靶點(diǎn)藥物中首個(gè)在宮頸癌、食管癌以及乳腺癌適應癥披露臨床有效性數據的品種。目前已開(kāi)展三項 III 期關(guān)鍵性注冊臨床。尿路上皮癌單藥、聯(lián)合特瑞普利單抗治療均被 CDE 納入突破性治療品種名單。并已被 FDA 授予 3 項快速通道認定(FTD)和 1 項孤兒藥資格認定(ODD)。
[1] Bray F, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2024;
[2] Zhang et al. ASCO 2024.
關(guān)于邁威生物
邁威生物 (688062.SH) 是一家全產(chǎn)業(yè)鏈布局的創(chuàng )新型生物制藥公司,始終秉承“讓創(chuàng )新從夢(mèng)想變成現實(shí)”的愿景,踐行“探索生命,惠及健康”的使命,通過(guò)源頭創(chuàng )新,為患者提供療效更好、可及性更強的生物創(chuàng )新藥,滿(mǎn)足全球未被滿(mǎn)足的臨床需求。2017 年成立以來(lái),邁威生物構建了以抗體藥物靶點(diǎn)發(fā)現與分子發(fā)現為起點(diǎn),覆蓋成藥性研究、臨床前研究、臨床研究和生產(chǎn)轉化等藥品研發(fā)全周期的創(chuàng )新體系,實(shí)現集研發(fā)、生產(chǎn)、營(yíng)銷(xiāo)于一體的全產(chǎn)業(yè)鏈布局。我們專(zhuān)注于腫瘤和年齡相關(guān)疾病,涉及腫瘤、自身免疫、骨疾病、眼科、血液、感染等治療領(lǐng)域,憑借國際領(lǐng)先的特色技術(shù)平臺和研發(fā)創(chuàng )新能力,建立了豐富且具有競爭力的管線(xiàn)。現有 16 個(gè)品種處于不同階段,包括 12 個(gè)創(chuàng )新品種和 4 個(gè)生物類(lèi)似藥,其中 4 個(gè)品種上市,1 個(gè)品種已提交上市許可申請前溝通(pre-NDA)會(huì )議申請,2 個(gè)品種處于 III 期關(guān)鍵注冊臨床階段。并獨立承擔 1 項國家“重大新藥創(chuàng )制”重大科技專(zhuān)項、2 項國家重點(diǎn)研發(fā)計劃和多個(gè)省市級科技創(chuàng )新項目。邁威生物以創(chuàng )新為本,注重產(chǎn)業(yè)轉化,符合中國 NMPA、美國 FDA、歐盟 EMA GMP標準的抗體和重組蛋白藥物產(chǎn)業(yè)化基地已在江蘇泰州投入使用,并已通過(guò)歐盟 QP 審計,位于上海金山和江蘇泰州的大規模商業(yè)化生產(chǎn)基地正在建設中。欲了解更多信息,請訪(fǎng)問(wèn):www.mabwell.com。
本新聞稿所發(fā)布的信息中可能會(huì )包含某些前瞻性表述。這些表述本質(zhì)上具有相當風(fēng)險和不確定性。在使用“預期”、“相信”、“預測”、“期望”、“打算”及其他類(lèi)似詞語(yǔ)進(jìn)行表述時(shí),凡與本公司有關(guān)的,目的均是要指明其屬前瞻性表述。本公司并無(wú)義務(wù)不斷地更新這些預測性陳述。
這些前瞻性表述乃基于本公司管理層在做出表述時(shí)對未來(lái)事務(wù)的現有看法、假設、期望、估計、預測和理解。這些表述并非對未來(lái)發(fā)展的保證,會(huì )受到風(fēng)險、不確性及其他因素的影響,有些乃超出本公司的控制范圍,難以預計。因此,受我們的業(yè)務(wù)、競爭環(huán)境、政治、經(jīng)濟、法律和社會(huì )情況的未來(lái)變化及發(fā)展的影響,實(shí)際結果可能會(huì )與前瞻性表述所含資料有較大差別。
本公司、本公司董事及雇員代理概不承擔 (a) 更正或更新本網(wǎng)站所載前瞻性表述的任何義務(wù);及 (b) 若因任何前瞻性表述不能實(shí)現或變成不正確而引致的任何責任。
(滑動(dòng)查看全部?jì)热荩?/strong>
0人